Associação Portuguesa de Investigação em Cancro
As células CAR-T no combate ao cancro - desafios atuais e oportunidades futuras
As células CAR-T no combate ao cancro - desafios atuais e oportunidades futuras
O estabelecimento da imunoterapia - estimulação do sistema imunitário para que este reconheça e destrua as células tumorais - como uma abordagem terapêutica eficaz no combate ao cancro, é, indubitavelmente, um dos maiores marcos no tratamento das doenças oncológicas dos últimos anos. Entre as várias classes disponíveis, como por exemplo, os anticorpos monoclonais inibidores dos checkpoints imunitários (Prémio Nobel da Medicina e Fisiologia em 2018), as terapias celulares com células T (Adoptive T cell therapies), nas quais se inserem as células CAR-T, constituem uma das terapêuticas imuno-oncológicas mais inovadoras. As células CAR-T derivam da modificação genética de células T fisiológicas, que passam a expressar, na membrana celular, um recetor quimérico de antigénio (CAR - chimeric antigen receptor) específico para um dado antigénio tumoral, tornando-se capazes de direcionar a sua atividade anti--tumoral endógena para os tumores alvo. A eficácia anti-tumoral desta tecnologia foi demonstrada em vários ensaios clínicos para o tratamento de cancros hematológicos (leucemias e linfomas), tendo sido aprovados em 2017, pela agência regulamentar norte-americana (FDA), e em 2018, pela agência regulamentar europeia (EMA), os dois primeiros produtos baseados em células CAR-T: KYMRIAH® da Novartis e YESCARTA® da Kite Pharma. Em Portugal, os ensaios clínicos com células CAR-T começam a dar os primeiros passos, quer no IPO do Porto, quer no IPO de Lisboa.
No entanto, o benefício clínico desta imunoterapia é ensombrado por efeitos secundários severos, na maioria das vezes letais. Para além deste facto, os resultados decorrentes da aplicação de células CAR-T no tratamento de tumores sólidos têm demonstrado baixa eficácia terapêutica, devido às barreiras físicas, químicas e imunossupressoras expostas pelo microambiente tumoral sólido, o que contrasta com o fácil acesso das células CAR-T aos cancros «líquidos», na corrente sanguínea.
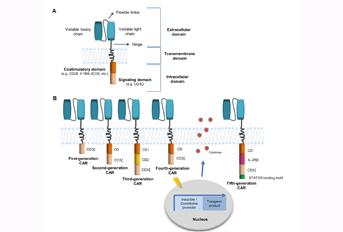
Neste contexto, o presente artigo de revisão, desenvolvido por investigadores pertencentes ao Centro de Neurociências e Biologia Celular (CNC) da Universidade de Coimbra, pretende ilustrar qual o panorama atual das terapias com células CAR-T em oncologia, focando-se nos mecanismos patofisiológicos subjacentes aos efeitos tóxicos reportados, bem como nas tecnologias CAR de última geração capazes de ultrapassar os problemas de segurança e eficácia atuais. Adicionalmente, este trabalho apresenta, de forma detalhada, os avanços clínicos mais recentes no âmbito do tratamento de tumores sólidos com células CAR-T, destacando quais as novas estratégias desenvolvidas para aumentar a sua atividade e persistência in vivo no tecido tumoral.
Autores e afiliações:
Teresa R. Abreu1,2, Nuno A. Fonseca1,3, Nélio Gonçalves1, João Nuno Moreira1,2
1CNC - Center for Neurosciences and Cell Biology, University of Coimbra, Faculty of Medicine (Polo 1), Rua Larga, 3004-504 Coimbra, Portugal
2FFUC - Faculty of Pharmacy, University of Coimbra, Pólo das Ciências da Saúde, Azinhaga de Santa Comba, 3000-548 Coimbra, Portugal
3TREAT U, SA, Parque Industrial de Taveiro, Lote 44, 3045-508 Coimbra, Portugal
Abstract:
Infusion of chimeric antigen receptor (CAR)-genetically modified T cells (CAR-T cells) have led to remarkable clinical responses and cancer remission in patients suffering from relapsed or refractory B-cell malignancies. This is a new form of adoptive T cell therapy (ACT), whereby the artificial CAR enables the redirection of T cells endogenous antitumor activity towards a predefined tumor-associated antigen, leading to the elimination of a specific tumor. The early success in blood cancers has prompted the US Food and Drug Administration (FDA) to approve the first CAR-T cell therapies for the treatment of CD19-positive leukemias and lymphomas in 2017. Despite the emergence of CAR-T cells as one of the latest breakthroughs of cancer immunotherapies, their wider application has been hampered by specific life-threatening toxicities, and a substantial lack of efficacy in the treatment of solid tumors, owing to the strong immunosuppressive tumor microenvironment and the paucity of reliable tumor-specific targets. Herein, besides providing an overview of the emerging CAR-technologies and current clinical applications, the major hurdles of CAR-T cell therapies will be discussed, namely treatment-related life-threatening toxicities and the obstacles posed by the immunosupressive tumor-microenvironment of solid tumors, as well as the next generation strategies currently designed to simultaneously improve safety and efficacy of CAR-T cell therapies in vivo.
Revista: Journal of Controlled Release
Link: https://authors.elsevier.com/c/1aMVwcI2~q0UJ






