Associação Portuguesa de Investigação em Cancro
Eficácia dos inibidores das HDACs Belinostat e Panobinostat no tratamento dos tumores de células germinativas do testículo sensíveis e resistentes à cisplatina
Eficácia dos inibidores das HDACs Belinostat e Panobinostat no tratamento dos tumores de células germinativas do testículo sensíveis e resistentes à cisplatina
Investigadores do Centro de Investigação do Instituto Português de Oncologia do Porto (IPO-Porto), do Grupo de Epigenética e Biologia do Cancro (GEBC), exploraram os efeitos in vitro de dois epi-fármacos (dois inibidores das desacetilases das histonas - HDACs) em linhas celulares de tumores de células germinativas do testículo, incluindo no contexto da resistência à cisplatina.
Os tumores de células germinativas do testículo são neoplasias muito heterogéneas, mas de uma maneira geral com boa resposta aos tratamentos disponíveis actualmente, nomeadamente devido à sensibilidade extrema à quimioterapia à base de cisplatina. Contudo, esta quimioterapia acarreta importantes efeitos laterais a longo prazo, com impacto na qualidade de vida destes doentes muito jovens. São, portanto, necessários novos tratamentos que complementem e potenciem a acção da cisplatina, de modo a permitir a redução da dose da mesma. Finalmente, um subgrupo de doentes desenvolve doença resistente à cisplatina e, à data, não existem tratamentos disponíveis para estes doentes, que eventualmente acabam por morrer da doença.
Neste trabalho, os investigadores usam uma série de tumores primários e metástases, incluindo tumores resistentes à cisplatina, e demonstram expressão diferencial de várias HDACs. Utilizando linhas celulares representativas destes tumores, incluindo clones isogénicos das mesmas onde foi induzida resistência à cisplatina (após cultura prolongada sob doses subletais de cisplatina), os autores demonstram que os dois mais recentes inibidores das HDACs aprovados pela FDA, Belinostat e Panobinostat, reduzem significativamente a viabilidade celular com doses baixas (IC50 abaixo de 1 micromolar).
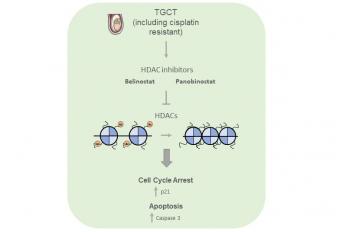
Ambos os fármacos promovem a apoptose, demonstrado através de ensaio fenotípico específico e através da indução da caspase clivada 3, e diminuem a proliferação celular destas linhas celulares, demonstrado através do ensaio BrdU e acompanhado pela diminuição do índice de proliferação (Ki67). Além disso, os autores confirmaram a acção dos fármacos sobre a acetilação, promovendo o aumento dos níveis de acetilação global e diminuindo a expressão de HDAC1. Em conclusão, os inibidores das HDACs são terapêuticas promissoras para doentes com tumores de células germinativas, incluindo no contexto de doença resistente à cisplatina.
Autores e Afiliações:
João Lobo 1,2,3,4,*, Catarina Guimarães-Teixeira 1,*, Daniela Barros-Silva 1, Vera Miranda-Gonçalves 1, Vânia Camilo 1, Rita Guimarães 1,2, Mariana Cantante 1,2, Isaac Braga 5, Joaquina Maurício 6, Christoph Oing 7, Friedemann Honecker 8, Daniel Nettersheim 9, Leendert HJ Looijenga 4, Rui Henrique 1,2,3,§,# and Carmen Jerónimo 1,3,§,#
1 Cancer Biology and Epigenetics Group, IPO Porto Research Center (GEBC CI-IPOP), Portuguese Oncology Institute of Porto (IPO Porto) & Porto Comprehensive Cancer Center (P.CCC), R. Dr. António Bernardino de Almeida, 4200-072, Porto, Portugal;
2 Department of Pathology, Portuguese Oncology Institute of Porto (IPOP), R. Dr. António Bernardino de Almeida, 4200-072, Porto, Portugal;
3 Department of Pathology and Molecular Immunology, Institute of Biomedical Sciences Abel Salazar, University of Porto (ICBAS-UP), Rua Jorge Viterbo Ferreira 228, 4050-513, Porto, Portugal
4 Princess Máxima Center for Pediatric Oncology, Heidelberglaan 25, 3584 CS Utrecht, The Netherlands;
5 Department of Urology, Portuguese Oncology Institute of Porto (IPOP), R. Dr. António Bernardino de Almeida, 4200-072, Porto, Portugal;
6 Department of Medical Oncology, Portuguese Oncology Institute of Porto (IPOP), R. Dr. António Bernardino de Almeida, 4200-072, Porto, Portugal;
7 Department of Oncology, Hematology and Bone Marrow Transplantation with Section of Pneumology, University Medical Center Hamburg-Eppendorf, Martinistraße 52, 20246 Hamburg, Germany & Laboratory of Radiation Biology and Experimental Radiation Oncology, University Medical Centre Hamburg-Eppendorf, Hamburg, Germany;
8 Department of Oncology, Hematology and Bone Marrow Transplantation with Section of Pneumology, University Medical Center Hamburg-Eppendorf, Martinistraße 52, 20246 Hamburg, Germany & Tumour and Breast Center ZeTuP St. Gallen, Rorschacher Strasse 150, 9006 St. Gallen, Switzerland; Friedemann;
9 Department of Urology, Urological Research Lab, Translational UroOncology, University Hospital Düsseldorf, 40225 Düsseldorf, Germany;
* joint first authors
§ joint senior authors
Abstract:
Novel treatment options are needed for testicular germ cell tumor (TGCT) patients, particularly important for those showing or developing cisplatin resistance, the major cause of cancer-related deaths. Because TGCTs pathobiology is highly related to epigenetic (de)regulation, epidrugs are potentially effective therapies. Hence, we sought to explore, for the first time, the effect of the two most recently FDA-approved HDAC inhibitors (HDACis) Belinostat and Panobinostat in (T)GCT cell lines, including those resistant to cisplatin. In silico results were validated in 261 patient samples and differential expression of HDACs was also observed across cell lines. Belinostat and Panobinostat reduced cell viability in both cisplatin-sensitive cells (NCCIT-P, 2102Ep-P and NT2-P) and, importantly, also in matched cisplatin-resistant subclones (NCCIT-R, 2102Ep-R and NT2-R), with IC50s in the low nanomolar range for all cell lines. Treatment of NCCIT-R with both drugs increased acetylation, induced cell cycle arrest, reduced proliferation, decreased Ki67 index and increased p21, while increasing cell death by apoptosis, with upregulation of cleaved caspase 3. These findings support the effectiveness of HDACis for treating TGCT patients in general, including those developing cisplatin resistance. Future studies should explore them as single or combination agents.
Revista: Cancers






